تالاسمی، یک بیماری ژنتیکی مادامالعمر است که هزینههای درمانی سنگینی را به خانوادهها و جامعه تحمیل میکند. با این وجود، افزایش آگاهی عمومی، به ویژه پیش از ازدواج، میتواند از تولد نوزادان مبتلا به این بیماری جلوگیری کند.
به گزارش پایگاه اطلاع رسانی جاده مخصوص، دکتر سعید دولتشاهی، فوق تخصص بیماریهای خون و سرطان، در گفتگویی با خبرآنلاین، تالاسمی را بیماری پرهزینهای دانست که با آگاهی میتوان از تولد نوزاد مبتلا به آن پیشگیری کرد. بسیاری از خانوادهها درباره بیماری تالاسمی ماژور، روشهای درمان و پیشگیری از آن سوالاتی دارند که دکتر دولت شاهی به برخی از آنها پاسخ داده است.
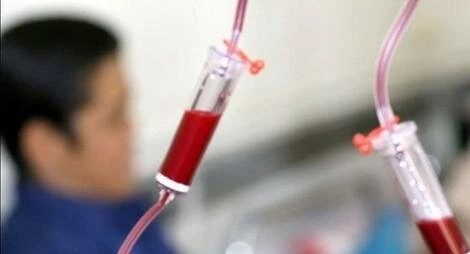
تزریق خون میتواند به دلایل مختلفی مانند سن، بیماریهای مزمن، شرایط حاد پزشکی یا جراحی انجام شود و تالاسمی تنها یکی از این دلایل است. پیوند مغز استخوان میتواند درمان قطعی تالاسمی ماژور باشد، اما مشروط به وجود دهنده سازگار و شرایط عمومی مناسب بیمار است. نارسایی کبد، بیماری قلبی، اعتیاد یا بیماریهایی مانند HIV میتوانند مانع انجام پیوند شوند. عوارض شدید ایمنی و عدم پذیرش پیوند توسط بدن نیز میتواند منجر به شکست درمان شود.
پیوند مغز استخوان ژنتیک فرد را تغییر نمیدهد و اگر مادر ناقل ژن تالاسمی باشد، حتی پس از پیوند نیز همچنان ناقل خواهد بود و در صورت ناقل بودن پدر، احتمال تولد نوزاد مبتلا به تالاسمی ماژور وجود دارد. با درمان منظم، شامل تزریق خون و مصرف داروهای کاهنده آهن، میانگین عمر بیماران تالاسمی میتواند به ۴۰ تا ۵۰ سال برسد. عدم پیگیری درمان میتواند منجر به عوارضی چون نارسایی قلبی، اختلالات کبدی، دیابت و کاهش طول عمر شود.
به گزارش جاده مخصوص، کمخونی مزمن و درمانهای مکرر میتواند بر میل جنسی و باروری تأثیر بگذارد و تالاسمی میتواند باعث کاهش میل جنسی، مشکلات روحی و روانی و کاهش باروری شود. با این حال، فرزندآوری برای این بیماران با مشاوره و مراقبتهای پزشکی امکانپذیر است. خانواده بیمار میتوانند خون اهدا کنند، اما خون اهدایی مستقیم به بیمار تزریق نمیشود و پس از طی مراحل تخصصی در بانک خون، آماده مصرف میشود.
دکتر دولت شاهی پیشگیری را بهترین درمان برای تالاسمی دانست و تاکید کرد که ابتلا به تالاسمی ماژور، علاوه بر خود فرد، خانواده و جامعه را نیز درگیر هزینهها، عوارض و فشارهای روانی میکند. پیشگیری از تولد نوزاد مبتلا، سادهترین، مؤثرترین و کمهزینهترین راهکار برای کنترل این بیماری است.
نظر شما در مورد این بیماری و روشهای پیشگیری از آن چیست؟ دیدگاه خود را در قسمت نظرات با ما به اشتراک بگذارید.